Très belle revue sur le covid long intitulée « Mechanisms of long COVID and the path toward therapeutics » de Peluso et Deeks.
Cette publication explore les mécanismes sous-jacents du long COVID, sa définition, ses implications épidémiologiques, et propose des axes de recherche pour développer des approches thérapeutiques.
1. Introduction et Définition du COVID Long
Le COVID long, également appelé PASC (séquelles post-aiguës du SARS-CoV-2), est un état chronique nouvellement identifié, associé à des symptômes persistants et inexpliqués suivant une infection par le SARS-CoV-2. Alors que la majorité des cas de COVID-19 se résolvent d’eux-mêmes, un pourcentage significatif de personnes infectées continue à souffrir de séquelles post-aiguës. Ces séquelles se manifestent de plusieurs façons : une faiblesse musculaire, de la fatigue, des troubles cognitifs, ainsi que des conditions médicales nouvellement développées ou aggravées telles que le diabète, des événements cérébrovasculaires ou des maladies auto-immunes.
Le COVID long affecte non seulement les patients ayant survécu à des formes graves de COVID-19, mais aussi un grand nombre de personnes ayant souffert de formes légères à modérées de la maladie. En fait, c’est cette dernière catégorie qui porte la charge la plus élevée du COVID long, bien qu’elles ne nécessitent souvent pas d’hospitalisation pendant la phase aiguë.
Définition du COVID Long
Il existe plusieurs définitions du COVID long, qui varient selon les organisations de santé. L’Organisation mondiale de la santé (OMS) définit cette condition comme des symptômes non expliqués persistant pendant au moins deux mois et apparaissant au moins trois mois après une infection au SARS-CoV-2. D’autres entités, telles que les Centres pour le contrôle et la prévention des maladies (CDC) aux États-Unis et le National Institute for Health and Care Excellence (NICE) au Royaume-Uni, utilisent des termes tels que « conditions post-COVID » ou « syndrome post-COVID ». En Espagne, une étude de consensus a défini cette condition comme un ensemble de symptômes multi-organiques qui persistent ou fluctuent après une infection aiguë.
Le terme long COVID a émergé au sein de la communauté des patients et est parfois utilisé pour désigner l’ensemble des séquelles liées au COVID-19. Aux États-Unis, un comité de l’Académie nationale des sciences a récemment défini le COVID long comme une « maladie chronique » diagnostiquée après trois mois de symptômes affectant un ou plusieurs systèmes organiques. Ces symptômes peuvent varier en gravité, être continus ou cycliques, et peuvent entraîner des handicaps socio-économiques importants.
Bien que les définitions varient, elles convergent autour de deux critères principaux : la durée des symptômes et l’inclusion de diagnostics médicaux nouveaux ou non expliqués après l’infection initiale.
2. Épidémiologie du COVID Long
L’épidémiologie du COVID long est complexe et varie selon les régions, les populations et les différentes vagues de variants du SARS-CoV-2. Les estimations de la prévalence du COVID long varient également en fonction des définitions utilisées. Certains travaux suggèrent qu’environ 30 % des personnes infectées développent des symptômes persistants, mais ces estimations incluent souvent des individus présentant des symptômes qui pourraient être dus à d’autres conditions. Il est donc essentiel d’exclure d’autres diagnostics comme des insuffisances cardiaques, des cancers ou des maladies thyroïdiennes avant de conclure à un COVID long.
De plus, il est difficile de distinguer les symptômes directement liés au COVID-19 de ceux résultant de conditions préexistantes ou non diagnostiquées auparavant. Toutefois, des études rigoureuses, telles que celles menées au sein du système de santé des anciens combattants aux États-Unis, montrent que les personnes ayant contracté le COVID-19 sont plus susceptibles de développer des complications à long terme, comparées à celles qui ont été infectées par d’autres virus comme la grippe. Ces complications touchent plusieurs systèmes organiques, notamment cardiovasculaires, neurologiques et rénaux.
Les estimations fiables indiquent qu’environ 18 millions d’adultes aux États-Unis souffriraient de symptômes persistants post-COVID. En mars 2023, une enquête menée au Royaume-Uni estimait que 2,9 % de la population présentait des symptômes du COVID long, dont 1,3 million de personnes ayant été infectées plus d’un an auparavant. De manière générale, environ 65 millions de personnes dans le monde seraient affectées par le COVID long, selon les projections de l’Institut pour la mesure et l’évaluation de la santé (IHME) et de l’OMS.
Facteurs de risque du COVID long
Les principaux facteurs de risque de développer le COVID long sont cohérents à travers les études : ils incluent le sexe féminin, l’âge avancé, la sévérité de l’infection aiguë et un statut socio-économique plus bas. Les études récentes suggèrent également que des facteurs génétiques et épigénétiques pourraient jouer un rôle.
Bien que les premières vagues du virus aient montré des taux d’incidence plus élevés du COVID long, la maladie persiste avec les nouveaux variants du virus, même après la généralisation de la vaccination et des traitements antiviraux. Les données sont encore incomplètes concernant les différences dans les risques de COVID long selon les variants, mais certaines études indiquent que le variant Omicron pourrait présenter un risque plus faible que les variants antérieurs, comme Delta. De même, la réinfection pourrait aggraver les symptômes du COVID long, même si les preuves sur ce point restent limitées.
Impact de la vaccination et des traitements
La vaccination contre le SARS-CoV-2 réduit le risque de développer un COVID long, mais elle ne l’élimine pas complètement. Les études montrent également que les traitements antiviraux administrés au début de l’infection aiguë peuvent réduire les risques de séquelles à long terme, bien que les résultats soient mitigés. Les traitements précoces visant à réduire la charge virale semblent jouer un rôle dans la prévention du COVID long, mais des recherches supplémentaires sont nécessaires pour évaluer l’efficacité des doses de rappel et des traitements prolongés dans la prévention des formes chroniques.
3. Caractéristiques Cliniques du COVID Long
Les symptômes du COVID long peuvent émerger pendant la phase aiguë de l’infection ou apparaître plus tard, souvent plusieurs semaines après l’infection initiale. Les symptômes les plus fréquents incluent la fatigue, des troubles cognitifs (souvent appelés « brouillard cérébral »), et des symptômes post-effort (c’est-à-dire une aggravation des symptômes après un effort physique ou mental). Ces symptômes peuvent fluctuer dans le temps, apparaissant par périodes, ou être continus.
De nombreux cas de COVID long présentent des symptômes liés à différents systèmes organiques. Par exemple, des symptômes cardiovasculaires, respiratoires, neurologiques, digestifs, musculo-squelettiques, et psychiatriques ont été rapportés. Certains patients souffrent de dysfonctionnements autonomiques, tels que le syndrome de tachycardie orthostatique posturale (POTS), caractérisé par une augmentation rapide de la fréquence cardiaque lors du passage à la position debout, provoquant des étourdissements et une fatigue importante.
3.1 Endotypes et Clusters Cliniques
Les études actuelles tentent de mieux comprendre les sous-types du COVID long, appelés « endotypes », en fonction des symptômes dominants. Par exemple, les essais cliniques RECOVER des National Institutes of Health (NIH) se concentrent sur des endotypes spécifiques, tels que la dysfonction autonome, l’altération neurocognitive, ou l’intolérance à l’exercice. L’identification de ces sous-types pourrait permettre de mieux cerner les mécanismes biologiques sous-jacents et d’adapter les traitements.
Des analyses récentes de dossiers de santé électroniques (DSE) ont permis d’identifier plusieurs clusters de symptômes, y compris des catégories cardio-rénales, respiratoires/sommeil/anxiété, musculo-squelettiques/neurologiques, et digestifs/respiratoires. Toutefois, l’hétérogénéité des symptômes rend difficile l’application pratique de ces sous-types dans le suivi clinique des patients.
3.2 Conditions Cliniques Connexes
Le COVID long présente également des similitudes avec d’autres conditions post-infectieuses chroniques, telles que le syndrome de fatigue chronique/encéphalomyélite myalgique (SFC/EM), la maladie de Lyme chronique, et le syndrome post-Ebola. Ces maladies ont historiquement reçu peu de ressources en raison des mêmes défis rencontrés dans l’étude du COVID long : scepticisme médical, absence de biomarqueurs clairs et diversité des symptômes.
3.3 Évolution des Symptômes
Dans la majorité des cas, les symptômes du COVID long s’améliorent progressivement au fil du temps. Cependant, chez certains patients, ces symptômes peuvent durer plusieurs mois, voire des années, provoquant un impact significatif sur la qualité de vie. Certains patients peuvent souffrir de handicaps physiques, cognitifs ou émotionnels durables, qui affectent leur capacité à travailler ou à mener des activités quotidiennes.
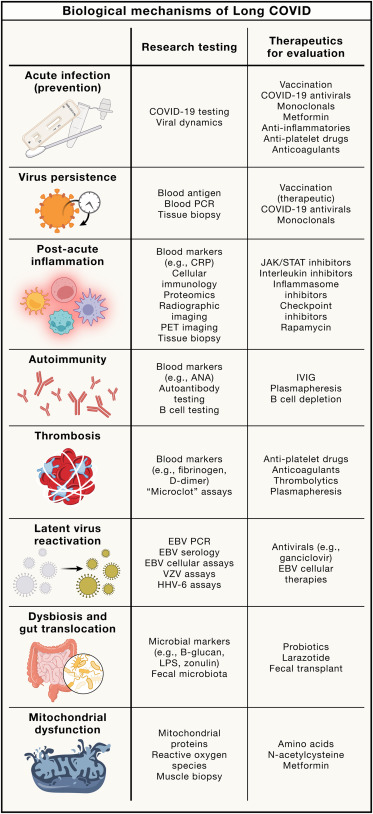
4. Mécanismes Biologiques / étiologie / les causes du COVID Long
Les mécanismes biologiques responsables du COVID long sont nombreux et souvent étudiés de manière isolée. Cependant, la biologie humaine est complexe, et il est probable que plusieurs de ces mécanismes soient interconnectés. Ils se divisent en deux grandes catégories : les mécanismes biologiques en amont, responsables de perturbations immunitaires, inflammatoires ou coagulationnelles, et les mécanismes physiologiques en aval, responsables des symptômes ressentis par les patients.
4.1 Conséquences de l’Infection Aiguë
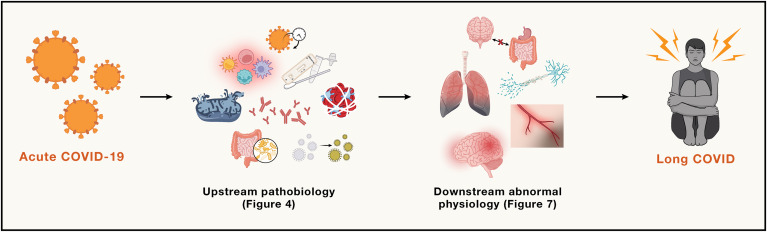
Le virus SARS-CoV-2 peut infecter plusieurs types de cellules, y compris les cellules épithéliales des voies respiratoires et les entérocytes du tractus gastro-intestinal. Il existe des preuves que des fragments de SARS-CoV-2, tels que la protéine Spike, peuvent persister dans l’organisme, notamment dans les tissus et organes affectés comme l’intestin, pendant des mois après l’infection initiale. Cela pourrait expliquer certains des symptômes persistants associés au COVID long.
Des études ont montré que la charge virale élevée pendant la phase aiguë de l’infection est liée à un risque accru de développer un COVID long. Par exemple, les patients ayant des charges virales plus élevées au début de l’infection ou ceux dont l’élimination du virus prend plus de temps sont plus susceptibles de présenter des symptômes persistants. Cependant, même les infections asymptomatiques peuvent parfois conduire au COVID long, suggérant que la réplication virale est un des facteurs contribuant au développement de la maladie.
4.2 Persistance Virale Post-Aiguë
L’idée que le SARS-CoV-2 puisse persister dans l’organisme bien après l’infection aiguë a été suggérée par la détection de l’ARN viral dans le sang, les tissus ou les excréments de patients plusieurs mois après leur guérison. Cette persistance pourrait expliquer certains des symptômes prolongés du COVID long. Cependant, il reste à clarifier si cette persistance virale est synonyme d’une infection active ou s’il s’agit de résidus viraux non infectieux.
Des études ont montré que des fragments viraux peuvent persister dans certains tissus, notamment dans le tube digestif, où l’ARN du SARS-CoV-2 a été détecté dans la muqueuse intestinale des patients souffrant de COVID long plus de deux ans après l’infection initiale. Cette persistance pourrait déclencher une réponse immunitaire continue, entraînant une inflammation chronique et d’autres symptômes systémiques.
4.3 Inflammation Post-Aiguë
Une autre hypothèse importante est celle d’une inflammation prolongée. Le COVID-19, particulièrement dans sa forme aiguë, induit une réponse inflammatoire importante. Certaines personnes développent une inflammation chronique qui persiste des mois après l’infection. Des marqueurs inflammatoires comme l’interleukine-6 (IL-6) et le TNF-alpha (facteur de nécrose tumorale) ont été associés à des symptômes de COVID long, notamment dans les formes neurologiques et cardiovasculaires.
La persistance d’une activation chronique des cellules immunitaires, comme les monocytes et les macrophages, pourrait également contribuer au COVID long, en maintenant une réponse inflammatoire anormale dans l’organisme. Certains patients présentent des signes de dysfonctionnement des cellules T (immunitaires), suggérant une stimulation immunitaire continue, soit par des résidus du virus SARS-CoV-2, soit par d’autres antigènes.
4.4 Activation des Mastocytes et Réponse Immunitaire Exagérée
Les mastocytes, qui ne sont pas directement infectés par le virus, peuvent être activés par diverses réactions immunitaires dans le corps. Ils libèrent alors des substances inflammatoires telles que l’histamine, qui peuvent provoquer des symptômes gastro-intestinaux, pulmonaires ou cutanés. Ce mécanisme pourrait expliquer certaines des similitudes entre les symptômes du COVID long et le syndrome d’activation mastocytaire, qui est une condition impliquant une hyperréactivité des mastocytes.
4.5 Autoimmunité
Certaines études suggèrent que l’infection par le SARS-CoV-2 pourrait déclencher des réponses auto-immunes, où le système immunitaire attaque les propres cellules et tissus du corps. Cela pourrait expliquer les symptômes persistants, notamment dans les cas où des anticorps auto-immuns sont détectés. Cependant, les preuves sur le rôle de l’auto-immunité dans le COVID long restent mitigées, et des recherches supplémentaires sont nécessaires pour établir une connexion claire.
4.6 Troubles de la Coagulation et Microclots
Une autre hypothèse propose que le COVID long est lié à des anomalies de la coagulation sanguine, notamment par la formation de microcaillots qui sont résistants à la dégradation. Ces microclots, associés à des protéines inflammatoires, pourraient obstruer les petits vaisseaux sanguins, entraînant des symptômes tels que la fatigue, des douleurs musculaires ou des troubles cognitifs en raison d’une mauvaise circulation sanguine dans les tissus.
5. Les mécanismes physiopathologiques qui expliquent les symptômes du long COVID.
5.1 le dommage aux organes :
- Hypothèse principale : Le long COVID pourrait être expliqué par des dommages directs causés aux tissus par l’infection virale initiale, qui persistent après la phase aiguë.
- Exemples : La fibrose pulmonaire post-COVID est un exemple classique de dommage tissulaire irréversible, causant des symptômes chroniques. Des dommages à d’autres organes, comme le pancréas (causant un diabète post-COVID), le cœur ou le cerveau, sont également rapportés.
- Conséquences : Si les symptômes sont dus à des dommages irréversibles, les traitements devront se concentrer sur des soins de soutien, la gestion des symptômes et la réhabilitation (physique et cognitive).
5.2. L’enjeu vasculaire : Endothéliopathie, thromboinflammation et hypoxie tissulaire
- Mécanismes : L’infection par le SARS-CoV-2 peut entraîner une inflammation de l’endothélium vasculaire (endothéliite) et des maladies microvasculaires. Cela peut mener à une dysfonction endothéliale, à la formation de microcaillots et à des processus thromboinflammatoires qui réduisent la perfusion des tissus.
- Conséquences : Cela peut entraîner une hypoxie tissulaire (réduction de l’apport en oxygène) et une dysfonction des organes, contribuant aux symptômes du long COVID.
- Observations : Des études ont montré des niveaux élevés et persistants de marqueurs de dysfonction endothéliale chez les personnes atteintes de long COVID. L’hypoperfusion tissulaire a également été observée lors de tests d’effort cardiopulmonaire et d’imagerie cérébrale.
5.3. Neuropathie et dysautonomie
- Modèle proposé : Le long COVID pourrait affecter le système nerveux périphérique, en particulier les petites fibres nerveuses qui régulent les fonctions motrices et sensorielles, ainsi que le système nerveux autonome (responsable des fonctions involontaires, comme le rythme cardiaque et la respiration).
- Symptômes : Cela peut entraîner des syndromes comme le POTS (syndrome de tachycardie orthostatique posturale), caractérisé par une augmentation de la fréquence cardiaque au passage à la position debout, ainsi que des symptômes comme la fatigue, les palpitations, les étourdissements et la douleur chronique.
- Mécanismes potentiels : La dysautonomie pourrait être causée par des dommages aux petites fibres nerveuses ou une auto-immunité, entraînant une altération du tonus vasculaire, une hypoperfusion systémique et une mauvaise régulation des réponses cardiaques.
5.4 Disruption of the gut-brain axis /Perturbation de l’axe intestin-cerveau)
- Hypothèse : L’infection par le SARS-CoV-2 pourrait perturber la communication bidirectionnelle entre l’intestin et le cerveau, notamment via l’axe hypothalamo-hypophyso-surrénalien (HPA), qui est un acteur clé dans la réponse au stress.
- Impact : La perturbation de cet axe pourrait être à l’origine de symptômes comme la fatigue, la dysfonction cognitive (brouillard cérébral) et des réponses anormales au stress, ainsi que d’une baisse des niveaux de cortisol observée chez certains patients atteints de long COVID.
- Mécanismes : La perturbation de l’équilibre du microbiote intestinal, causée par l’infection, pourrait avoir des effets sur la neurotransmission et les signaux neurochimiques envoyés au cerveau, exacerbant les symptômes neurocognitifs.
5.5 Sickness behavior and energy preservation (Comportement de maladie et conservation de l’énergie)
- Théorie : Le long COVID pourrait entraîner un « comportement de maladie » prolongé, une réponse évolutive qui pousse le corps à économiser de l’énergie pour faire face à l’infection. Ce comportement inclut une réduction des activités physiques et mentales, une consommation calorique réduite et une baisse des fonctions reproductives.
- Syndrome de fatigue chronique : Cette réponse prolongée est souvent observée dans des maladies comme le syndrome de fatigue chronique (SFC), ce qui pourrait suggérer une analogie avec le long COVID.
Ces différents mécanismes physiopathologiques montrent que le long COVID n’est pas seulement lié à une cause unique, mais résulte probablement d’une interaction complexe de plusieurs processus : dommages directs aux organes, inflammation chronique, perturbation du système nerveux, dysfonction endothéliale et hypoxie, ainsi que la réactivation d’infections latentes. Ces modèles physiopathologiques fournissent des cibles potentielles pour le développement de traitements, bien que davantage de recherche soit nécessaire pour relier précisément ces mécanismes aux symptômes spécifiques du long COVID.
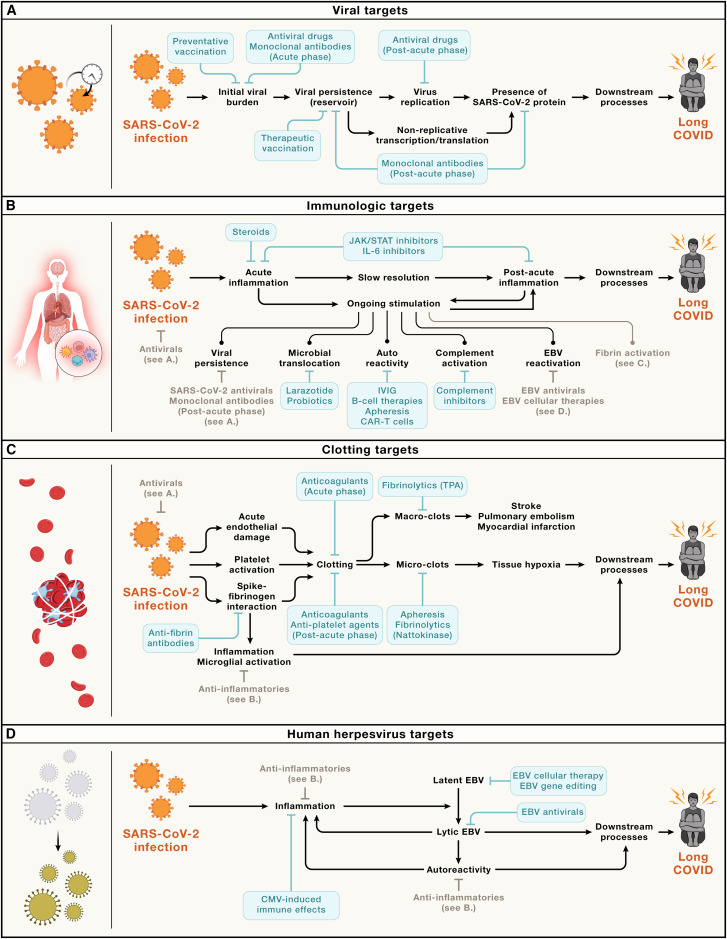
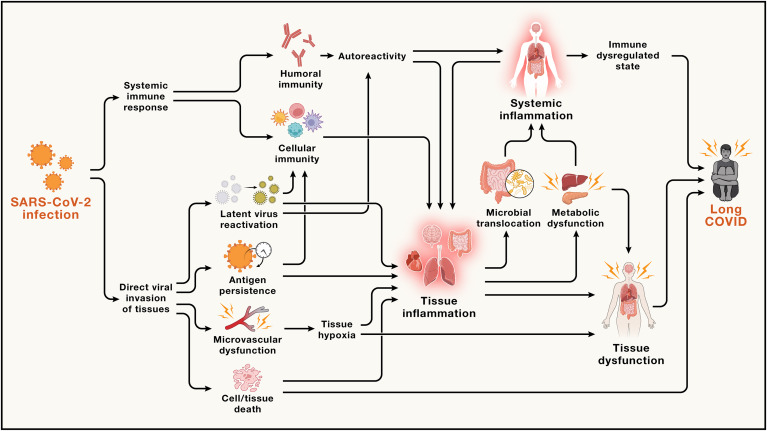
6. APPROCHES THERAPEUTIQUES
La section Therapeutic Approaches » se concentre sur les différentes approches thérapeutiques envisageables pour le traitement du COVID long. Voici une synthèse rigoureuse des points principaux couverts :
6.1 Antiviraux
- Objectif : Limiter la persistance du virus SARS-CoV-2 chez les patients atteints de COVID long. L’idée sous-jacente est que certains symptômes pourraient être dus à la présence résiduelle du virus dans certains tissus, même après la phase aiguë.
- Antiviraux envisagés : Des médicaments tels que le nirmatrelvir/ritonavir et d’autres antiviraux comme le molnupiravir ou le remdesivir sont étudiés pour prévenir la réactivation du virus ou réduire les réservoirs viraux potentiels dans les tissus. Cependant, les résultats des premiers essais sont mitigés, certains montrant peu de différence avec un placebo dans l’amélioration des symptômes du COVID long.
6.2 Modulateurs immunitaires
- Rôle de l’inflammation : L’une des principales hypothèses pour expliquer le COVID long est la réponse inflammatoire persistante qui entraîne une dysfonction immunitaire. Des traitements qui ciblent cette inflammation sont donc prometteurs.
- Traitements potentiels : Des thérapies ciblant des molécules spécifiques de l’inflammation (cytokines) sont à l’étude, comme des inhibiteurs de l’IL-6, des inhibiteurs de la JAK/STAT (tels que le baricitinib), et d’autres agents immunomodulateurs comme le tocilizumab. Des essais de ces médicaments sont en cours ou planifiés pour évaluer leur efficacité sur les symptômes du COVID long.
6.3 Thérapies anti-thrombotiques
- Microthromboses : Des études ont montré que des microthromboses (petits caillots sanguins) pourraient être responsables des dysfonctionnements vasculaires observés chez certains patients atteints de COVID long.
- Traitements anticoagulants : Des thérapies anticoagulantes et antiplaquettaires, comme l’aspirine ou le clopidogrel, ont été testées chez des patients atteints de COVID long présentant des signes de microclots, avec certains résultats prometteurs. Toutefois, ces approches nécessitent des études contrôlées pour confirmer leur efficacité à long terme.
6.4 Immunothérapie et auto-immunité
- Auto-immunité : Le COVID-19 sévère est associé à l’auto-immunité, et certains patients atteints de COVID long montrent également des signes d’auto-anticorps. Des thérapies visant à réduire la production d’auto-anticorps ou à moduler la réponse immunitaire adaptative sont envisagées.
- Inhibiteurs de points de contrôle : Pour les patients présentant des signes d’épuisement immunitaire, l’utilisation d’inhibiteurs de points de contrôle pourrait être une approche thérapeutique potentielle pour restaurer la capacité du système immunitaire à éliminer les réservoirs viraux.
6.5 Thérapies ciblant les réactivations virales latentes
- Réactivation de l’EBV (virus Epstein-Barr) : Une réactivation de l’EBV a été observée chez de nombreux patients atteints de COVID long. Des traitements antiviraux visant spécifiquement ces virus latents, en plus du SARS-CoV-2, pourraient être envisagés dans des essais cliniques.
6.6 Stratégies combinées
- Combinaison des traitements : Il est probable que le COVID long résulte de mécanismes multiples et imbriqués, rendant nécessaire une approche thérapeutique combinée. Par exemple, cibler simultanément la persistance virale, la dysfonction immunitaire et les microthromboses pourrait être plus efficace que des thérapies isolées.
L’approche thérapeutique du COVID long est complexe, car elle doit traiter une multitude de mécanismes physiopathologiques potentiels, allant de la persistance virale à l’inflammation chronique en passant par les dysfonctionnements vasculaires et immunitaires. De nombreux essais cliniques sont en cours pour tester différentes thérapies, mais une meilleure compréhension des mécanismes spécifiques du COVID long est nécessaire pour affiner les traitements disponibles.
7. Le Chemin vers les essais cliniques
7.1 Ralentissement dans le développement des essais cliniques
- Il est souligné que malgré la reconnaissance des mécanismes physiopathologiques du long COVID et l’identification de cibles thérapeutiques, la mise en place d’essais cliniques a été lente.
- Il y a encore trop peu d’essais cliniques bien dimensionnés, et très peu se concentrent sur les mécanismes proposés qui sous-tendent le long COVID.
7.2 Considérations essentielles pour les essais cliniques
- Les essais doivent désormais être orientés par les résultats des études mécanistiques pour cibler de manière rationnelle les patients présentant des symptômes spécifiques liés aux mécanismes biologiques identifiés.
- L’inclusion de la dimension du sexe est essentielle, car les femmes (notamment les femmes préménopausées) semblent plus susceptibles que les hommes de développer le long COVID. Des différences biologiques dans la réponse immunitaire selon le sexe pourraient être en jeu, influençant la conception des essais et le ciblage thérapeutique.
7.3 Importance des hormones sexuelles
- Il existe des preuves que des niveaux réduits de testostérone chez les hommes et d’œstrogène chez les femmes peuvent jouer un rôle dans la persistance des symptômes du long COVID.
- Ces hormones sont liées à des réponses immunitaires plus fortes chez les femmes, ce qui pourrait expliquer en partie pourquoi elles sont plus touchées par certaines maladies auto-immunes et chroniques, y compris le long COVID.
Le chemin vers des essais cliniques efficaces pour le long COVID est encore entravé par un manque de financement et de coordination, bien que des progrès soient réalisés. Les études futures devront mieux prendre en compte les différences biologiques et hormonales entre les sexes, et il est impératif que les cibles thérapeutiques soient définies sur la base des découvertes mécanistiques du long COVID.
7.4 Essais cliniques combinés
- Les essais cliniques sur le long COVID pourraient nécessiter une accélération, en particulier lorsqu’il s’agit de combiner des traitements. Ces combinaisons pourraient viser plusieurs mécanismes à la fois, tels que la persistance virale, les dysfonctionnements de la coagulation, ou l’inflammation immunitaire.
- Il est probable que les thérapies simples ne seront pas suffisantes pour traiter le long COVID en raison de sa nature multi-mécanistique. Par exemple, combiner un antiviral pour réduire la charge virale et un agent anticoagulant pour prévenir la formation de caillots pourrait offrir des avantages supplémentaires.
7.5 Mécanismes multi-niveaux
- Le long COVID implique plusieurs niveaux de perturbations biologiques et physiologiques. Il est donc suggéré que des essais cliniques doivent cibler non seulement les causes « en amont » (comme la persistance du virus), mais aussi les conséquences physiologiques « en aval », telles que la dysfonction endothéliale ou les perturbations de l’axe intestin-cerveau.
7.6 Cheminement vers les essais combinés
- Traditionnellement, les essais cliniques commencent par tester des thérapies individuelles contre un placebo avant de combiner les traitements qui montrent des résultats positifs. Cependant, dans le cas du long COVID, la progression vers des essais combinés pourrait devoir être accélérée afin d’apporter des solutions plus rapidement.
La section souligne l’importance d’accélérer les essais cliniques combinant plusieurs traitements afin de mieux cibler les multiples mécanismes sous-jacents au long COVID. Ces essais doivent être conçus de manière à intervenir sur plusieurs fronts, y compris les effets viraux et immunitaires, pour maximiser l’efficacité des traitements.
Conclusions
Cette section souligne la gravité du défi posé par le long COVID, comparable en ampleur à celui de la pandémie de COVID-19 elle-même. Le long COVID est décrit comme une maladie complexe, affectant potentiellement des millions de personnes à travers le monde. Bien qu’il y ait des parallèles avec d’autres conditions inflammatoires et auto-immunes chroniques, le long COVID se distingue par l’ampleur des individus touchés simultanément, tous ayant été exposés au même agent pathogène.
- Nécessité urgente de la recherche :
- Il est urgent de mener des recherches approfondies sur plusieurs fronts, y compris l’épidémiologie, la biologie fondamentale, la science translationnelle, les essais cliniques, et la science de la mise en œuvre. Cette approche permettra d’acquérir une compréhension complète de l’histoire naturelle du long COVID, de ses mécanismes biologiques et des traitements potentiels.
- Efforts de recherche interdisciplinaires :
- La section encourage la collaboration à grande échelle entre des disciplines variées pour développer des biomarqueurs, des tests fonctionnels, et des interventions cliniques spécifiques au long COVID. Ces efforts devraient être coordonnés à l’échelle internationale, comme cela a été fait pour les vaccins et les traitements pour le COVID aigu.
- Conséquences à long terme et pour d’autres conditions :
- Les investissements dans la recherche sur le long COVID peuvent également bénéficier à d’autres conditions inflammatoires et post-infectieuses similaires, y compris celles qui ont historiquement reçu moins d’attention. La recherche sur le long COVID pourrait ainsi avoir des impacts positifs bien au-delà de la pandémie actuelle et préparer le terrain pour de futures pandémies ou infections similaires.
Le long COVID est une condition majeure qui nécessite une réponse scientifique urgente et coordonnée. Il existe un besoin critique de comprendre ses mécanismes sous-jacents, de développer des traitements efficaces, et de mieux soutenir les millions de personnes touchées.
Référence : Peluso, M. J., & Deeks, S. G. (2024). Mechanisms of long COVID and the path toward therapeutics. Cell, 187(1), 17-28. https://doi.org/10.1016/j.cell.2024.07.054



Laisser un commentaire